Dr. Pablo Riera Arévalo
Médico Cirujano Urólogo
Rut: 14.654.981-0 Médico Cirujano Universidad Nacional De Cuyo, Argentina. Médico Cirujano Universidad de Chile. Urología Universidad de Valparaíso. Jefe de Servicio de Urología, Transplante Renal y Procura Hospital Dr. Gustavo Fricke.
Atiende enViña del Mar
Temas de Urología
- Anatomía Sistema Urinario
- Cáncer de Riñón
- Circuncisión
- Cistitis intersticial
- Hidrocele y hernia inguinal
- Infecciones del tracto urinario
- Tratamiento quirúrgico de la incontinencia urinaria
- Tratamiento quirúrgico del cáncer de próstata
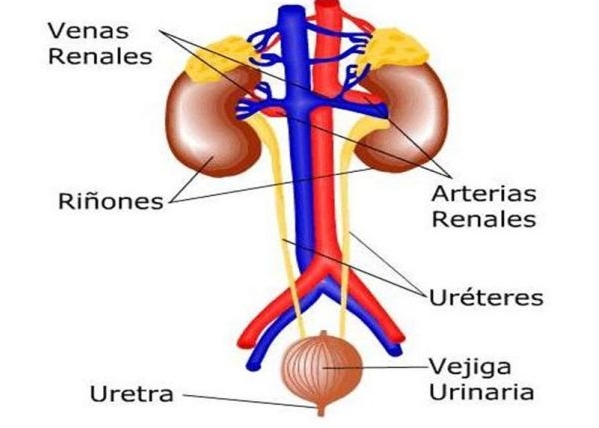
¿Cómo funciona el sistema urinario? El cuerpo toma las sustancias nutritivas de los alimentos y las convierte en energía. Después de que el cuerpo ha tomado los alimentos que necesita, deja productos de desecho en el intestino y en la sangre. El sistema urinario mantiene los productos químicos y el agua en equilibrio eliminando un tipo de desecho de la sangre llamado urea. La urea se produce cuando la proteína, que se encuentra en los productos cárnicos, se descompone en el cuerpo. Las partes del sistema urinario y sus funciones: Dos riñones: un par de órganos de color oscuro entre café y morado, situados debajo de las costillas y hacia el medio de la espalda. Su función es: - Eliminar los desechos líquidos de la sangre en forma de orina. - Mantener un equilibrio estable de sales y otras sustancias en la sangre. - Producir eritropoyetina, una hormona que ayuda en la formación de los glóbulos rojos. Los riñones: eliminan la urea de la sangre a través de unas unidades de filtración diminutas llamadas nefronas. Cada nefrona consiste en una bola formada por pequeños capilares sanguíneos llamados glomérulos y por un pequeño tubo llamado túbulo renal. La urea, junto con el agua y otras sustancias de desecho, forma la orina al pasar a través de las nefronas y bajar a los túbulos renales. Dos uréteres: tubos estrechos que llevan la orina de los riñones a la vejiga. Los músculos de las paredes de los uréteres se contraen y relajan continuamente para forzar la orina hacia abajo, lejos de los riñones. Si la orina se acumula, o si se queda sin moverse, puede desarrollarse una infección del riñón. Aproximadamente cada 10 ó 15 segundos, los uréteres vacían cantidades pequeñas de orina en la vejiga. Vejiga: órgano hueco de forma triangular, situado en el abdomen inferior. Está sostenida por ligamentos unidos a otros órganos y a los huesos de la pelvis. Las paredes de la vejiga se relajan y dilatan para acumular la orina, y se contraen y aplanan para vaciarla a través de la uretra. La vejiga típica del adulto sano puede almacenar hasta dos tazas de orina en un período de dos a cinco horas. Dos músculos del esfínter: músculos circulares que ayudan a que la orina no gotee cerrándose herméticamente como una cinta de goma alrededor del orificio de la vejiga. Nervios de la vejiga: avisan a la persona cuando es hora de orinar o de vaciar la vejiga. Uretra: tubo a través del cual pasa la orina desde la vejiga al exterior del cuerpo. El cerebro envía señales a los músculos de la vejiga para que se contraigan y expulsen la orina. Al mismo tiempo, el cerebro envía señales a los músculos del esfínter para que se relajen y permitan la salida de orina de la vejiga a través de la uretra. Cuando todas las señales se suceden en el orden correcto, ocurre la micción normal. Los adultos eliminan cada día aproximadamente un litro y medio de orina, según el consumo de líquidos y alimentos. El volumen de orina formado por la noche es aproximadamente la mitad del formado durante el día. Datos acerca de la orina: La orina normal es estéril. Contiene líquidos, sales y productos de desecho, pero no tiene bacterias, virus ni hongos. Los tejidos de la vejiga están aislados de la orina y de las sustancias tóxicas por medio de una capa que no permite que las bacterias se adhieran y crezcan en la pared de la vejiga.
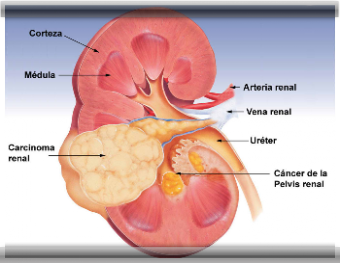
Cáncer de Riñon
Es importante darse cuenta que el cáncer de riñón puede curarse si se diagnostica y trata a tiempo. Si se detecta precozmente, la tasa de supervivencia para pacientes con cáncer de riñón varía entre el 79 y el 100 por ciento. La siguiente información responde las preguntas más comunes acerca de los tumores que afectan a los riñones y sirve como complemento a la charla que debe tener con su médico. ¿Qué es un tumor renal? Un tumor renal es un crecimiento anormal dentro del riñón. A menudo los términos “masa”, “lesión” y “tumor” se usan como sinónimos. Los tumores pueden ser benignos (no cancerosos) o malignos (cancerosos). La lesión renal más común es la presencia de un área llena de líquido llamada quiste. Los quistes simples son benignos y tienen un aspecto típico en los estudios por imágenes. No progresan al cáncer y normalmente no requieren seguimiento ni tratamiento. Los tumores sólidos de riñón pueden ser benignos, pero en más del 90 por ciento de las veces son cancerosos. ¿Qué factores de riesgo se asocian con el cáncer de riñón? Las siguientes asociaciones pueden aumentar el riesgo de desarrollar cáncer de riñón: * fumar. * antecedente familiar de cáncer de riñón. * poliquistosis renal. * insuficiencia renal crónica, diálisis, o ambas. * dieta con alta ingesta de calorías o carnes fritas o salteadas. * baja ingesta de vitamina E. * uso de diuréticos. * enfermedad de von Hippel-Lindau. * esclerosis tuberosa. * exposición a asbestos, altos hornos y hornos usados en la industria del hierro y el acero. ¿Cuáles son los síntomas del cáncer de riñón? Muchos tumores de riñón no producen síntomas, pero pueden ser detectados accidentalmente durante la evaluación por algún otro problema no relacionado. La compresión, estiramiento e invasión de las estructuras cerca de los riñones pueden causar dolor (en el flanco, en el abdomen o en la espalda), la presencia de una masa palpable y sangre en la orina (microscópica o visible a simple vista). Si el cáncer se disemina (metástasis) más allá del riñón, los síntomas dependerán del órgano afectado. Si el cáncer compromete a los pulmones puede observarse falta de aire o tos con sangre, si el cáncer involucra a los huesos puede ocurrir que haya dolor en los huesos o fracturas, y si el cáncer se presenta en el cerebro puede haber síntomas neurológicos. En algunos casos el cáncer causa alteraciones clínicas o de laboratorio asociadas llamadas síndrome paraneoplásico. Este síndrome se observa aproximadamente en un 30 por ciento de los pacientes con cáncer de riñón y pueden ocurrir en cualquier etapa (y esto incluye a los cánceres confinados a los riñones). Los síntomas del síndrome paraneoplásico incluyen la pérdida de peso, la pérdida del apetito, la presencia de fiebre, sudoración y aumento de la tensión arterial. Los análisis de laboratorio determinan una tasa de sedimentación de glóbulos rojos alta, bajo recuento de glóbulos rojos (anemia), alto nivel de calcio en sangre, alteración de las pruebas de función hepática, alto contenido de fosfatasa alcalina en la sangre, y alto recuento de glóbulos blancos. En muchos casos el síndrome paraneoplásico se resuelve luego de resecar el cáncer. ¿Cómo se diagnostica el cáncer de riñón? Desafortunadamente no hay análisis de sangre ni de orina que puedan detectar directamente la presencia de un tumor de riñón. Cuando se sospecha la presencia de un tumor de riñón se hace un estudio por imágenes del órgano. El primer estudio por imágenes normalmente es una ecografía o una tomografía computarizada. En algunos casos puede ser necesaria una combinación de estudios por imágenes para evaluar el tumor por completo. Si se sospecha el diagnóstico de cáncer, el paciente debe ser evaluado para determinar si el cáncer se ha diseminado más allá de los riñones (metástasis). La evaluación para detectar metástasis incluye una tomografía computarizada o una RM de la región abdominal, radiografías de tórax y análisis de sangre. También se recomienda una centellografía ósea si el paciente tiene dolor en los huesos, si ha sufrido alguna fractura recientemente, o si presenta ciertas alteraciones en los análisis de sangre. Es posible que se indiquen también más análisis de ser necesario. El cáncer de riñón tiene la tendencia a crecer dentro de la vena renal y de la vena cava. La porción del cáncer que se extiende a estas venas se denomina “trombo tumoral”. Los estudios por imágenes ayudan a determinar si existe un trombo tumoral. ¿Cuáles son las opciones de tratamiento para tumores que parecen estar confinados al riñón? Cuando el tumor parece estar confinado al riñón (tumor “localizado”), hay tres opciones principales de tratamiento: - Resección del tumor. - Ablación del tumor. - Vigilancia. La quimioterapia, el tratamiento hormonal y la radioterapia no son tratamientos eficaces para el cáncer de riñón. Resección del tumor: La resección del tumor se considera el modo estándar de tratamiento para la mayoría de los pacientes y se logra mediante una cirugía llamada nefrectomía. Una nefrectomía radical es la resección quirúrgica de todo lo que se encuentre dentro de la fascia de Gerota, incluido el riñón completo. La nefrectomía parcial es la resección quirúrgica de parte del riñón (en este caso, la parte que contiene el tumor). El objetivo de una nefrectomía parcial es resecar el tumor completo y a la vez preservar la mayor cantidad posible de tejido renal normal. El tejido renal que se conserva puede evitar la necesidad de diálisis si ocurre un mayor daño renal posteriormente. Es posible realizar la nefrectomía mediante una incisión tradicional (cirugía a cielo abierto) o con pequeñas incisiones (cirugía laparoscópica o retroperitoneoscópica). Nefrectomía a cielo abierto (radical y parcial): La nefrectomía tradicional a cielo abierto (parcial o radical) se realiza mediante una incisión en el flanco o en el abdomen. Esta incisión normalmente mide entre 10 y 20 pulgadas de longitud (25,4 – 50,8 cm) y puede incluir la remoción de una costilla. Antes se consideraba que la nefrectomía radical a cielo abierto era el tratamiento de elección para tumores que parecían estar confinados al riñón. Sin embargo, los seguimientos a 5 a 10 años pusieron en evidencia que las nefrectomías parciales y radicales a cielo abierto son igualmente eficaces para el tratamiento de pacientes con un único tumor pequeño y localizado. Por lo tanto, las nefrectomías parciales y radicales se consideran en la actualidad como el tratamiento estándar. Si está interesado en una nefrectomía parcial, es importante que consulte a un urólogo que tenga experiencia con esta técnica. Como se mencionó anteriormente, la nefrectomía parcial se realiza para preservar la mayor cantidad posible de tejido renal; sin embargo, la tasa de complicaciones puede ser levemente superior que la de la nefrectomía radical. Debe considerarse realizar una nefrectomía parcial abierta en pacientes que tengan un tumor pequeño (lo ideal es que tengan menos de cuatro centímetros) y localizado en uno de los riñones y un riñón normal del otro lado. La nefrectomía parcial a cielo abierto normalmente es el tratamiento de preferencia cuando se espera que la nefrectomía radical resulte en diálisis inmediata o en un alto riesgo de diálisis subsiguiente, como cuando el paciente tiene un solo riñón funcional, o una función renal muy deteriorada, o enfermedades médicas o genéticas que amenazan la función renal, o tumores de riñón bilaterales. Normalmente no se recomienda una nefrectomía parcial en pacientes con tumores que tienen al menos una de las siguientes características: diseminación dentro de la vena renal, proximidad a los vasos principales del riñón o factores que harían que una resección completa del tumor sea poco probable. Cuando no es posible resecar con seguridad el tumor con una nefrectomía parcial, se realiza una nefrectomía radical. Si elige someterse a una nefrectomía parcial, siempre existe el riesgo de que haya necesidad de resecar todo el riñón. Nefrectomía radical laparoscópica: La nefrectomía laparoscópica se realiza mediante el uso de telescopios que se insertan en la cavidad abdominal a través de pequeñas incisiones como si fueran un “ojo de cerradura”; sin embargo, a menudo se hace una incisión algo más grande para permitir la resección de un riñón entero. Las nefrectomías que se realizan mediante la inserción de los telescopios en la cavidad que rodea al riñón (y no en la cavidad abdominal) se denominan nefrectomías retroperitoneoscópicas. Los datos actuales indican que las nefrectomías radicales a cielo abierto y las laparoscópicas tienen tasas de complicaciones similares y proporcionan un tratamiento eficaz contra el cáncer en pacientes cuyos tumores parecen estar confinados al riñón. En comparación con la nefrectomía radical a cielo abierto, la nefrectomía radical laparoscópica se prolonga por más tiempo, es menos dolorosa luego de la operación, el período de hospitalización es más corto y requiere menos tiempo de recuperación. Si elige someterse a una nefrectomía radical laparoscópica, hay un bajo riesgo (normalmente menos del cinco por ciento) de que el cirujano tenga que pasar a una nefrectomía a cielo abierto (es decir, convertir las incisiones de “ojo de cerradura” en una incisión mucho más grande). No todos los pacientes son candidatos para una nefrectomía laparoscópica. La nefrectomía radical laparoscópica es más adecuada para tumores pequeños y localizados que no han invadido los ganglios linfáticos ni la vena renal. En pacientes con cicatrización importante alrededor del riñón o el antecedente de varias cirugías abdominales se prefiere la nefrectomía a cielo abierto. Los cirujanos que tienen experiencia con la retroperitoneoscopia pueden considerar la realización de este abordaje en pacientes que han sido sometidos a varias cirugías abdominales. Nefrectomía parcial laparoscópica y retroperitoneoscópica: Se está acumulando información acerca de la nefrectomía parcial laparoscópica y la retroperitoneoscópica, pero los datos sobre las complicaciones y el control del cáncer son aún prematuros. Ablación del tumor: La ablación del tumor destruye el tumor sin extirparlo quirúrgicamente. Entre los ejemplos de las diferentes tecnologías que se pueden aplicar para la ablación se incluye la crioterapia, la ablación intersticial por radiofrecuencia, el ultrasonido localizado de alta intensidad, la termoterapia por microondas y la coagulación con láser. La ablación puede lograrse durante una cirugía a cielo abierto, una laparoscopia, una retroperitoneoscopia o de manera percutánea (a través de la piel). Como la ablación de un tumor renal es un procedimiento relativamente nuevo, todavía no se sabe cuáles son los resultados a largo plazo. Sin embargo, la ablación puede ser menos invasiva que una nefrectomía y puede ser útil en los pacientes que no pueden tolerar cirugías más extensas. La ablación del tumor también puede permitir una mejor probabilidad de preservar la función renal en situaciones en las que hay varios tumores. Embolización: Ésta no es una opción estándar de tratamiento, pero puede considerarse en pacientes que no pueden tolerar la resección o la ablación del tumor. También puede considerarse como un tratamiento coadyuvante a las formas estándar de tratamiento, especialmente cuando el tumor presenta sangrado activo. La embolización puede detener el sangrado y permite al médico estabilizar al paciente antes de la cirugía. La embolización normalmente se hace bajo sedación y se logra al hacer avanzar un catéter largo y delgado desde una arteria periférica (por ejemplo, en la ingle) hasta la arteria del riñón. El catéter se utiliza para depositar pequeñas partículas de material embólico en los vasos del riñón. Estas partículas bloquean el flujo de sangre al tumor y, por lo tanto, detienen el sangrado activo. Más aún, sin suministro de sangre, el tumor es muy probable que muera. Como no está claro si la embolización elimina el tumor por completo o no, no se considera una forma primaria de tratamiento para el cáncer de riñón. ¿Cuáles son las opciones de tratamiento para los tumores que se han diseminado a otros órganos? Cuando el tumor se ha diseminado a otros órganos, hay cuatro opciones de tratamiento primario: nefrectomía seguida de inmunoterapia, tratamiento inicial con inmunoterapia, estudios clínicos de investigación y vigilancia. Inmunoterapia: La inmunoterapia estimula al sistema inmunológico para que éste ataque al cáncer. El sistema inmunológico con suerte eliminará al cáncer de la misma manera como se elimina una gripe. Los agentes que más habitualmente se utilizan para la inmunoterapia son la interleucina-2 (IL-2) y el interferón. Actualmente, la IL-2 es el único tratamiento eficaz aprobado por la Food and Drug Administration (FDA; Administración de Alimentos y Fármacos) para el tratamiento del cáncer metastásico de riñón. Aproximadamente un 20 por ciento de los pacientes responden a la inmunoterapia con algún grado de regresión del tumor. Aproximadamente el 7 por ciento de los pacientes presentan una regresión total del cáncer. Se ha estudiado muchos regímenes diferentes de inmunoterapia. Uno de los más eficaces es una dosis alta de IL-2 en bolo, para lo que se requiere internación en el hospital. Durante la internación hospitalaria inicial se administra IL-2 por vía intravenosa durante cinco días. El paciente luego normalmente puede ir a su hogar para descansar por un período de entre cinco y 10 días. Luego el paciente se interna nuevamente para otro ciclo de IL-2 intravenosa durante cinco días. Los efectos secundarios más comunes son muy similares a los síntomas de la gripe e incluyen fiebre, escalofríos, náuseas, vómitos, diarrea y fatiga. Otros efectos secundarios incluyen la disminución de la tensión arterial, la acumulación de líquido en los pulmones (edema pulmonar), el deterioro de la función hepática, el deterioro de la función renal, las alteraciones del estado mental (como confusión, agitación, ciclo de sueño interrumpido), el aumento de la frecuencia cardíaca y el ritmo cardíaco irregular. La mayoría de los efectos secundarios son transitorios y desaparecen al suspender la inmunoterapia. Para ser un candidato a la inmunoterapia el paciente debe estar en un buen estado general, debe tener una función adecuada de los órganos vitales (como el corazón, los pulmones y los riñones) y no debe tener metástasis en el cerebro. La inmunoterapia no es eficaz contra los cánceres que se localizan en el cerebro. Antes de la inmunoterapia, los pacientes deben hacerse estudios para evaluar la función de los órganos vitales y una tomografía para determinar si hay metástasis en el cerebro. Nefrectomía seguida de inmunoterapia: En los pacientes con metástasis, la mejor posibilidad de supervivencia se logra mediante la resección del riñón afectado antes de administrar la inmunoterapia. El riñón puede resecarse mediante cirugía a cielo abierto o cirugía laparoscópica. Esta opción de tratamiento sólo se ofrece cuando el paciente es candidato tanto para la nefrectomía como para la inmunoterapia. Por lo tanto, los pacientes no deben ser sometidos a ningún tratamiento hasta no haber sido evaluados tanto por un oncólogo que se especialice en inmunoterapia como por un cirujano urológico. El tratamiento sólo debe iniciarse luego de que el cirujano y el oncólogo aprueban al paciente como candidato tanto a la nefrectomía como a la inmunoterapia. Tratamiento inicial con inmunoterapia: En algunos pacientes, la cirugía puede ser muy riesgosa. Estos pacientes pueden ser tratados inicialmente con inmunoterapia. Si responden adecuadamente y si su estado médico mejora, pueden ser sometidos a una resección quirúrgica del tumor restante. Estudios clínicos de investigación: No todos los pacientes tienen acceso a los protocolos de investigación. Si le interesa averiguar más acerca de estos protocolos, consulte con su médico, averigüe en la institución académica cercana o busque en Internet. Hay muchos tratamientos no estandarizados que se están analizando en estudios de investigación. Algunos de estos tratamientos incluyen la inmunoterapia celular, las vacunas contra el tumor, la terapia génica, los trasplantes de células madre, el tratamiento anti-angiogénesis, los inhibidores de los factores de crecimiento, etc. Aunque estos tratamientos parecen promisorios, todavía son experimentales y no está claro si son eficaces para el cáncer de riñón o no. Radiación: La radioterapia no se usa para curar el cáncer de riñón, sino más bien para aliviar las metástasis sintomáticas. Por ejemplo, el dolor de la metástasis en los huesos puede aliviarse mediante la irradiación de las lesiones óseas. Puede aplicarse sola o en combinación con otros tratamientos. Vigilancia: Puede ser apropiada cuando se está en presencia de una de las siguientes situaciones: el tumor del riñón tiene una baja probabilidad de ser cáncer; el paciente no tolera el tratamiento; el paciente tiene una expectativa de vida corta (es decir, es probable que fallezca por otras causas); o el paciente no quiere recibir tratamiento. En el caso de lesiones cuya probabilidad de ser cáncer es baja, es indispensable el seguimiento periódico con un médico. El angiomiolipoma, que es un tumor benigno y es el único tumor de riñón que puede ser diagnosticado por tomografía computarizada. Los pacientes con angiomiolipoma pueden ser sometidos a vigilancia con la realización periódica de estudios por imágenes. Sin embargo, puede ser necesario realizar una embolización o resección quirúrgica (preferiblemente mediante una nefrectomía parcial) si el angiomiolipoma es sintomático, si sangra o si mide más de cuatro centímetros.
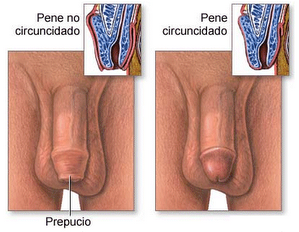
Circuncisión
La circuncisión, es decir la remoción del prepucio del pene, que se realiza en los bebés recién nacidos (neonatos) tiene beneficios potenciales y ventajas médicas así como desventajas y riesgos.
La circuncisión neonatal es, por lo general, un procedimiento rápido y seguro cuando la hace un médico con experiencia. Hay riesgos inmediatos de la circuncisión, como el sangramiento, la infección y la lesión peniana, así como complicaciones reconocidas más adelante que pueden incluir un pene encarcelado, estenosis del meato, puentes cutáneos y mal aspecto estético. Algunas de estas complicaciones pueden requerir corrección quirúrgica. No obstante, cuando la circuncisión se realiza en lactantes recién nacidos sanos como procedimiento de elección, la incidencia de complicaciones graves es extremadamente baja. Las complicaciones menores tienen una incidencia del tres por ciento.
Hay una relación entre el prepucio y las infecciones del tracto urinario. Durante los primeros tres a seis meses de vida, la incidencia de infecciones del tracto urinario es al menos diez veces mayor en los niños no circuncidados que en los circuncidados. La evidencia que relaciona la circuncisión con una menor incidencia de las enfermedades de transmisión sexual es discutida. Puede ser necesario realizar la circuncisión en una pequeña cantidad de niños no circuncidados cuando ocurren fimosis, parafimosis o balanopostitis recurrente, y puede ser solicitada por razones étnicas y culturales luego del período inmediato posterior al nacimiento. La circuncisión en estos niños normalmente requiere anestesia general.
Al discutir el tema de la circuncisión con los padres y para la firma del consentimiento informado, deben considerarse los beneficios y los riesgos médicos, así como cuestiones étnicas, culturales, religiosas y preferencias individuales. Los riesgos y las desventajas de la circuncisión se encuentran al poco tiempo de realizado el procedimiento, mientras que las ventajas y los beneficios pueden ser a futuro.

Cistitis Intersticial
La cistitis intersticial (CI) es una enfermedad crónica que afecta a la vejiga. Sus síntomas son la necesidad urgente de orinar (la sensación de necesitar orinar), necesidad de orinar frecuentemente y/o dolor en cualquier lugar entre el ombligo y la parte interior de los muslos, por delante o por detrás. Los síntomas varían desde leves a severos, y pueden ser intermitentes o constantes. Los casos más graves de CI pueden tener un efecto devastador tanto sobre quien la sufre como sobre sus seres queridos.
En el pasado se creía que la CI era una enfermedad rara que era muy difícil de tratar. En la actualidad se sabe que la CI afecta a una gran cantidad de hombres y mujeres. La siguiente información lo ayudará a discutir esta enfermedad con su urólogo y a comprender cuáles son los tratamientos que se encuentran disponibles.
¿Qué ocurre en condiciones normales?
Una vez que la orina es producida en los riñones, desciende por los uréteres hasta la vejiga. La vejiga es un órgano hueco similar a un globo. La mayor parte de las paredes de la vejiga está compuesta por músculo. A medida que la vejiga se llena, el músculo se relaja para que la vejiga se pueda expandir para contener la orina. Durante la evacuacion de la orina, el músculo de la vejiga se contrae para expulsar la orina. Para pasar desde la vejiga hacia el exterior, la orina es conducida a través de un tubo que se llama uretra. La uretra tiene un músculo, el esfínter, que es completamente diferente del músculo de la vejiga. El esfínter normalmente permanece cerrado y se sella para evitar que la orina salga de la vejiga. Durante la evacuacion el esfínter se abre y permite que la orina pase.
La vejiga y la uretra tienen una cubierta especializada que se denomina epitelio. El epitelio forma una barrera entre la orina y el músculo de la vejiga. El epitelio también evita que las bacterias se peguen a la vejiga, por lo que ayuda de esta manera a evitar infecciones en la vejiga.
¿Qué es la cistitis intersticial (CI)?
La CI es una enfermedad inflamatoria crónica de la vejiga que también puede afectar a la uretra y a la próstata. Los síntomas pueden ser leves o severos, ocasionales o constantes. No es una infección, pero los síntomas pueden parecerse a los de una infección de la vejiga.
¿Cuáles son algunos de los factores de riesgo para la CI?
No hay comportamientos específicos ni exposiciones (como el tabaco) que se sepa que aumentan el riesgo de una persona a desarrollar CI. La tendencia a contraer CI puede estar influenciada por los genes de la persona, o si tienen un pariente consanguíneo con CI. Alrededor del 90 por ciento de las personas a las que se les diagnostica CI son mujeres, lo que sugiere que este grupo tiene un mayor riesgo de desarrollar CI. Sin embargo, la diferencia en las tasas de CI para el sexo masculino en comparación con el sexo femenino puede en realidad no ser tan grande como se piensa, porque algunos hombres con diagnóstico de “prostatitis” u otra enfermedad similar con diferente nombre pueden en realidad tener CI.
¿Cuántas personas tienen CI en los Estados Unidos?
Es difícil saber a ciencia cierta cuántas personas tienen CI, debido a que los médicos tienen diferentes opiniones acerca de cómo se debe diagnosticar exactamente la CI.
¿Cuáles son las causas de la CI?
Las causas de la CI se están estudiando en diferentes centros médicos en todo el mundo. Muchos investigadores creen que la CI está causada por uno o más de los siguientes factores: (1) un defecto en el epitelio de la vejiga que permite que ciertas sustancias irritantes de la orina penetren la pared de la vejiga; (2) un tipo específico de células inflamatorias (mastocitos) que liberan histaminas u otros agentes químicos que promueven los síntomas de la CI en la vejiga; (3) hay algo en la orina que daña la vejiga; (4) los nervios que transportan las sensaciones a la vejiga están modificados, lo que hace que eventos que normalmente no son dolorosos causen dolor (como el llenado de la vejiga); y/o (5) el sistema inmunológico del cuerpo ataca a la vejiga, de manera similar a lo que ocurre en otras enfermedades autoinmunes. Es probable que en diferentes grupos de pacientes ocurran diferentes procesos. También es probable que estos diferentes procesos se afecten entre ellos (por ejemplo, un defecto en el epitelio de la vejiga puede promover la inflamación y estimular a los mastocitos). Algunos estudios de investigación recientes han demostrado que los pacientes con CI pueden tener una sustancia en la orina que inhibe el crecimiento de las células del epitelio vesical. Por lo tanto, algunas personas pueden tener una predisposición a desarrollar CI luego de una lesión en la vejiga, como ser una infección.
¿Cuáles son los síntomas de la CI?
Los síntomas de la CI varían de acuerdo al paciente. Si usted tiene CI, puede experimentar un aumento de la frecuencia urinaria y sensación de urgencia para orinar o dolor, o ambos. Muchas personas sólo tienen dolor pero no aumento de la frecuencia urinaria, aunque la mayoría de los pacientes con CI presentan todos los síntomas. Ha habido muchos casos informados cuando una persona diagnosticó con IC no experimentaba el dolor substancial.
El aumento de la frecuencia es la necesidad de orinar más a menudo que lo normal. Normalmente, una persona promedio orina no más de siete veces al día, y no necesita levantarse durante la noche para ir al baño. Un paciente con CI necesita orinar con frecuencia, tanto de día como de noche. A medida que la frecuencia empeora, se convierte en urgencia. La urgencia para orinar es un síntoma habitual de la CI. Algunos pacientes sienten una urgencia constante que nunca pasa, incluso después de orinar. Si bien otros pacientes con CI orinan a menudo, no necesariamente sienten esta urgencia para ir al baño todo el tiempo.
Los pacientes con CI pueden sufrir de dolor en la vejiga que empeora a medida que la vejiga se llena. Algunos pacientes con CI sienten el dolor en otras áreas además de la vejiga. Una persona puede sentir dolor en la uretra, en la región inferior del abdomen, en la región inferior de la espalda o en el área de la pelvis o perineal. Las mujeres pueden experimentar dolor en la vulva o en la vagina, y los hombres pueden sentir dolor en el escroto, en los testículos o en el pene. El dolor puede ser constante o intermitente.
Muchos pacientes con CI pueden identificar ciertas cosas que empeoran los síntomas. Por ejemplo, los síntomas de algunas personas empeoran al ingerir ciertas comidas o bebidas. Muchos pacientes encuentran que los síntomas son peores si tienen estrés (ya sea estrés físico o mental). Los síntomas pueden variar con el ciclo menstrual. Tanto los hombres como las mujeres con CI pueden experimentar dificultades sexuales a causa de esta enfermedad; las mujeres pueden sufrir dolor durante el coito porque la vejiga se encuentra al frente de la vagina, y los hombres pueden sentir dolor en el orgasmo o dolor al día siguiente.
¿Cómo se diagnostica la CI?
Actualmente hay diferentes opiniones acerca de cómo se diagnostica la CI. Esto se debe a que por ahora ninguna prueba ha resultado ser completamente precisa. Todos los médicos están de acuerdo en que para la evaluación se necesita contar con una buena historia de los sintomas, el examen físico y análisis de orina. Estas pruebas son importantes para descartar otras enfermedades que puedan estar causando los síntomas. Algunos médicos creen que se está en presencia de CI si el paciente tiene los síntomas de CI y no se puede encontrar ninguna otra causa para explicar esos síntomas. Sin embargo, otros médicos creen que se necesitan más estudios para determinar si el paciente tiene CI.
Uno de estos exámenes que muchos médicos utilizan es una cistoscopia simple realizada en el consultorio, en la que el médico mira dentro de la vejiga con un cistoscopio sin aplicar anestesia. Este examen puede descartar otras enfermedades, como el cáncer. Mientras que la cistoscopia es un examen sencillo que puede realizarse en el consultorio del médico, hay un examen más invasivo que se puede realizar en la sala de operaciones. Incluye un examen cistoscópico simple seguido de un estrechamiento o distensión de la vejiga, lo que se logra introduciendo agua bajo presión. De esta manera se pueden poner en evidencia hendiduras en la vejiga en los casos más severos.
Hace un tiempo la cistoscopia era parte de la evaluación usual para el diagnóstico de CI, pero ya no se considera siempre necesaria para esta enfermedad porque el estudio suele ser normal. Sin embargo, durante la cistoscopia algunos pacientes presentarán pequeñas áreas de sangrado, o verdaderas úlceras, que el médico puede observar con el cistoscopio. Las úlceras normalmente se encuentran sólo en los pacientes que tienen más de 60 años de edad y a menudo se puede sospechar de su existencia por la presencia de sangre en la orina. Si una persona tiene síntomas de CI y la cistoscopia muestra sangrado o úlceras, el diagnóstico es bastante exacto. La mayoría de las personas que tienen síntomas de CI no presentan estas áreas sangrantes, pero igualmente pueden tener CI y tal vez respondan a los mismos tratamientos. El médico entonces a menudo realizará una biopsia de la vejiga, que ayuda a descartar otras enfermedades vesicales. Si bien este procedimiento se utiliza principalmente para hacer estudios, algunos pacientes con CI pueden experimentar un alivio de los síntomas luego de hacerlo. Algunos médicos creen que si una persona tiene los síntomas típicos de la CI y no se encuentra ninguna otra causa que explique los síntomas, entonces el paciente tiene CI. Esta sigue siendo un área de controversia que probablemente se podrá resolver con futuros estudios de investigación.
La evaluación urodinámica es otro estudio que hace un tiempo se consideraba parte de la evaluación estándar para determinar la presencia de CI pero que ya no se cree que sea necesaria en todos los casos. Este estudio requiere que la vejiga se llene con agua mediante un pequeño catéter que permite medir las presiones vesicales cuando la vejiga se llena y cuando se vacía. Los resultados habituales cuando se está en presencia de CI indican que la vejiga tiene poca capacidad y tal vez se experimenta dolor con el llenado.
Algunos médicos utilizan una prueba llamada prueba de la sensibilidad al potasio, para la que se introduce en la vejiga, una a la vez, una solución de potasio y agua y se comparan las graduaciones de dolor y necesidad imperiosa de orinar. Una persona que tiene CI siente más dolor o necesidad imperiosa de orinar con la solución de potasio que con el agua, pero los pacientes con vejiga normal no pueden diferenciar las dos soluciones.
Actualmente no hay una respuesta definitiva acerca de la mejor forma para diagnosticar la CI. Sin embargo, si un paciente tiene los síntomas típicos y un análisis de orina que indica que no hay infección ni sangre, se debe sospechar la presencia de CI.
¿La CI se desarrolla en etapas?
La CI es una enfermedad que a menudo comienza de una forma sutil, habitualmente con una mayor frecuencia para orinar que el paciente puede no notar o no reconocer como un problema. En otros casos, el inicio es mucho más drástico y los síntomas severos se presentan en un lapso de semanas o meses. En muchos casos, los síntomas se vuelven crónicos pero la enfermedad no tiende a progresar luego de los primeros 12 a 18 meses. Muy ocasionalmente, la vejiga se tornará cada vez más pequeña hasta llegar a un punto en el que ya casi no tenga capacidad para almacenar orina.
¿Cómo es el tratamiento de la CI?
No se conocen las causas de la CI. Como probablemente haya diferentes causas, no hay un único tratamiento que funcione para todos los pacientes, y ningún tratamiento es “el mejor”. El tratamiento debe elegirse individualmente para cada paciente en función de sus síntomas. Normalmente se prueban diferentes tratamientos (o combinaciones de tratamientos) hasta que ocurra el alivio de los síntomas.
Actualmente hay dos tratamientos aprobados por la Administración de Fármacologicos y Alimentos de los Estados Unidos (United States Food and Drug Administration, FDA) para tratar la CI. Uno es el pentosano polisulfato. No se sabe a ciencia cierta exactamente cómo actúa sobre la CI. Muchos piensan que construye y restaura el revestimiento protector del epitelio de la vejiga. También puede ayudar al reducir la inflamación o por medio de otros efectos. La dosis habitual es de 100 mg tres veces al día. Es muy poco común que tenga efectos secundarios, y si los hay, los más comunes son náuseas, diarrea y malestar gástrico. A menudo se necesitan entre tres y seis meses de tratamiento con pentosano polisulfato por vía oral antes de que el paciente note una mejora importante en los síntomas.
El otro tratamiento aprobado por la FDA es colocar dimetil sulfóxido (DMSO) en la vejiga con la ayuda de una sonda. Esto normalmente se hace una vez a la semana durante seis semanas, y algunas personas continúan utilizándolo como tratamiento de mantenimiento (aunque con intervalos más largos de tiempo y no todas las semanas).
No se sabe a ciencia cierta cómo actúa el DMSO sobre la CI. Tiene varias propiedades, entre las que se incluye el bloqueo de la inflamación, la disminución de la sensación de dolor y la eliminación de un tipo de toxinas llamadas “radicales libres” que pueden dañar a los tejidos. Algunos médicos combinan el DMSO con otros medicamentos como la heparina (similar al pentosano polisulfato) o esteroides (para reducir la inflamación). No hay estudios que hayan probado si estas combinaciones funcionan mejor que el dimetil sulfóxido solo. El principal efecto secundario del DMSO es un olor semejante al del ajo que dura durante varias horas luego de la aplicación. Para algunos pacientes, la introducción del DMSO en la vejiga puede ser dolorosa. A menudo se puede aliviar este dolor aplicando antes anestesia local en la vejiga mediante una sonda, o mezclando el anestésico local con el DMSO.
Hay una amplia variedad de otros tratamientos que se usan para la CI, aunque no están específicamente aprobados por la FDA para este propósito. Los más comunes son la hidroxicina por vía oral, la amitriptilina también por vía oral, y la introducción de heparina en la vejiga con la ayuda de una sonda.
La hidroxicina es una medicina antihistamínica. Se cree que algunos pacientes con CI tienen demasiada histamina en la vejiga, y que la histamina promueve el dolor y los otros síntomas. Por lo tanto, el uso de antihistamínicos puede ser útil en el tratamiento de la CI.
La dosis habitual es de 10 a 75 mg por la noche. El principal efecto secundario es la sedación, pero esto en realidad puede ser beneficioso porque ayuda al paciente a dormir mejor por la noche y a levantarse con menos frecuencia para orinar. Los únicos antihistamínicos que se han estudiado específicamente para la CI son la hidroxicina y (más recientemente) la cimetidina. No se sabe si hay otros antihistamínicos que puedan ser útiles para tratar la CI.
La amitriptilina se describe como una medicina antidpresiva, pero en realidad tiene muchos efectos que pueden mejorar los síntomas de la CI. Tiene efectos antihistamínicos, disminuye los espasmos de la vejiga, y reduce la conducción por los nervios que transportan los mensajes de dolor (por ese motivo se utiliza para muchos tipos de dolor, no sólo para la CI). La amitriptilina es frequentemente usada para otros tipos de dolores crónicos como el cáncer y lesións de los nervios. La dosis habitual es de 10 a 75 mg por la noche. Los efectos secundarios más comunes son la sedación, la constipación, y un posible aumento de peso.
La heparina es similar al pentosano polisulfato y probablemente ayude a la vejiga mediante mecanismos similares. La heparina no es absorbida por el estómago y las inyecciones a largo plazo pueden causar osteoporosis (debilitación de los huesos), y por lo tanto debe ser colocada en la vejiga mediante una sonda. La dosis habitual es de 10.000 a 20.000 unidades diarias o tres veces a la semana. No suele presentar efectos secundarios porque la heparina permanece sólo en la vejiga y normalmente no afecta al resto del cuerpo.
También se usan muchos otros tratamientos contra la CI, pero con menos frecuencia que los que se describieron aquí. Algunos pacientes no responden a ningún tratamiento para esta enfermedad pero aún así pueden lograr una mejoría importante en su calidad de vida gracias a un tratamiento adecuado del dolor. El tratamiento adecuado del dolor puede incluir el uso de medicinas antiinflmatorias, narcoticos de potencia moderada y narcoticos más potentes de acción prolongada además del bloqueo de nervios, la acupuntura y otros tratamientos sin medicinas. El tratamiento profesional del dolor a menudo puede ser útil en los casos más severos.
¿Qué se puede esperar luego del tratamiento de la CI?
Lo más importante que se debe recordar es que ninguno de los tratamientos contra la CI es de acción inmediata. Normalmente se necesitan semanas o meses para lograr una mejoría de los síntomas. Incluso con un tratamiento exitoso, la enfermedad no se “cura”, simplemente se encuentra “en etapa de remisión”.
La mayoría de los pacientes debe continuar el tratamiento indefinidamente para evitar que los síntomas recurran. Algunos pacientes sufren una reagudización de los síntomas incluso cuando todavía están bajo tratamiento.
Si bien la mayoría de los pacientes notará que sus síntomas mejoran a medida que continúan el tratamiento de la CI, no todos los pacientes podrán liberarse por completo de los síntomas. Muchos pacientes continúan con la necesidad de orinar con más frecuencia que lo normal, o sufren algún grado de incomodidad persistente y/o deben evitar ciertos alimentos o actividades que hacen empeorar los síntomas.
¿Es posible que la CI recurra después de un tratamiento exitoso? ¿Cómo se pueden evitar las recurrencias?
Es posible que los síntomas de la CI recurran incluso si la enfermedad ha estado en remisión por mucho tiempo. No se sabe cuáles son las causas de las recurrencias. Tampoco hay una forma segura de prevenir las recurrencias. Algunas de las cosas que los pacientes pueden hacer para prevenir la recurrencia incluyen: (1) continuar con el tratamiento médico incluso luego de la remisión; (2) evitar ciertos alimentos que puedan irritar la vejiga; y (3) evitar ciertas actividades o estrés que puedan empeorar la CI. Los alimentos o actividades específicas que afectan la CI son diferentes para cada paciente, por lo que cada persona debe armar su propio plan individual.
Preguntas frecuentes:
¿Cómo se ve afectada la CI por la dieta?
La mayoría de las personas (pero no todas) con CI encuentran que ciertos alimentos hacen empeorar los síntomas. Hay cuatro alimentos que los pacientes a menudo encuentran irritantes para la vejiga: cítricos, tomates, chocolate y café. Estos cuatro alimentos son ricos en potasio. Otros alimentos que incomodan la vejiga en muchos pacientes son las bebidas alcohólicas, las comidas muy condimentadas y algunas bebidas carbonatadas. La lista de alimentos que se ha informado afecta la CI es bastante extensa, pero no todos los alimentos afectan a todos los pacientes de la misma manera. Por este motivo, cada paciente debe determinar cómo estos alimentos afectan a su vejiga.
La forma más sencilla de determinar si un alimento afecta a la vejiga o no es hacer una “dieta de eliminación” durante una o dos semanas. Para hacer la dieta de eliminación debe dejar de comer todos los alimentos que puedan irritar la vejiga. Las listas de alimentos para la CI pueden buscarse en diferentes sitios (www.ichelp.org o www.ic-network.com). Si los síntomas de la vejiga mejoran durante la dieta de eliminación, esto quiere decir que al menos uno de los alimentos estaba irritando su vejiga.
El siguiente paso es determinar exactamente qué alimentos le están causando problemas en la vejiga a usted. Luego de una o dos semanas de hacer la dieta de eliminación, intente incorporar uno de los alimentos de la lista de alimentos para la CI. Si dentro de las 24 horas de ingerirlo no siente molestias en la vejiga, el alimento probablemente sea seguro y lo puede volver a incorporar a su dieta normal. Al otro día, intente incorporar un segundo alimento de la lista, y siga con el mismo procedimiento para todos los demás. De esta forma, incorporará nuevamente los alimentos a su dieta de a uno por vez, y los síntomas de su vejiga le dirán si alguno de esos alimentos le causa problemas. Asegúrese de agregar sólo un nuevo alimento a su dieta cada día. Si una persona ingiere bananas, frutillas y tomates todo el mismo día y esa noche los síntomas de la CI empeoran, no podrá saber cuál de los tres alimentos hizo que se manifestara el síntoma.
¿El estrés causa CI?
Actualmente no hay evidencia de que el estrés haga que una persona desarrolle CI. Sin embargo, es bien conocido ` que si una persona ya tiene CI, el estrés físico o mental puede hacer que los síntomas empeoren.
¿La CI es hereditaria?
Hay investigaciones que indican que existe un patrón genético. Es importante discutir los síntomas de la CI con la familia, especialmente las mujeres, de manera que los otros familiares afectados puedan controlarse y recibir tratamiento en las etapas iniciales de la enfermedad.
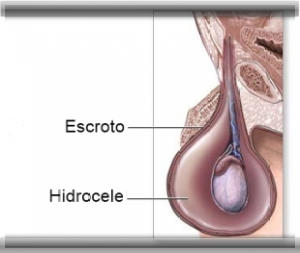

Hidrocele y Hernia Inguinal
Los hidroceles y las hernias inguinales (ubicadas en la ingle) pueden causar problemas en los hombres.
¿Pueden causan dolor o molestia?
¿Cuándo y cómo deben tratarse?
La siguiente información debería resultarle útil para hablar con un urólogo acerca de estas dos enfermedades.
¿Cuál es la causa de las hernias y de los hidroceles?
Los testículos se desarrollan cerca de los riñones en el abdomen y desde allí descienden a su posición normal en el escroto hacia el final del embarazo. Para que los testículos salgan del abdomen, hay un anillo muscular a cada lado de la ingle que se abre y permite que los testículos bajen al escroto. A medida que el testículo desciende, es acompañado por la capa que tapiza al abdomen también desciende para revestir el escroto. En la mayoría de los niños este canal se cierra. Si el canal permanece abierto o se vuelve a abrir, una pequeña cantidad de fluido puede pasar del abdomen al escroto a través de este pasaje, pudiendo formar un hidrocele. Si el canal permanece abierto o se vuelve a abrir mucho, entonces puede pasar una porción del intestino por el canal hacia el escroto, pudiendo formar una hernia inguinal.
Los hidroceles también se pueden desarrollar a causa de una inflamación o una lesión dentro del escroto. A veces sanan en unos pocos meses, pero muchos permanecen y requieren de atención médica. Las hernias también pueden ser el resultado de una mayor presión que hace que parte de los intestinos pase a través de un punto débil de la pared abdominal: como el esfuerzo al defecar, levantar objetos pesados, toser, estornudar o la obesidad.
¿Cuáles son los síntomas de una hernia?
Sólo un 25 por ciento de las hernias causan dolor o algún tipo de malestar. Sin embargo, es posible que vea y sienta el bulto que a menudo se produce en la unión entre el muslo y la ingle. Alrededor de un 1 por ciento de los niños desarrollan hernias, y la incidencia es mayor en lactantes prematuros del sexo masculino. A veces el intestino que protruye entra al escroto y causa dolor, hinchazón o abultamiento en el escroto, o ambos.
¿Cuáles son los síntomas de un hidrocele?
Alrededor del 10 por ciento de los lactantes del sexo masculino presentan un hidrocele en el momento del nacimiento. Este hinchazón o abultamiento del escroto rara vez causa síntomas, no molesta al bebé y normalmente desaparece durante el primer año de vida, si bien su presencia puede preocupar a los padres. En los varones de mayor edad, los hidroceles normalmente son indoloros pero puede causar alguna molestia debido al aumento del volumen del escroto.
¿Cómo se trata una hernia?
En los niños que presentan una hernia causada por el anillo muscular que no se cerró adecuadamente, se recomienda el tratamiento quirúrgico. Las hernias no desaparecen solas y pueden ocasionar problemas digestivos que pueden conducir a una cirugía de emergencia. En los lactantes y niños se hace una pequeña incisión en la ingle, a través de la cual el urólogo sutura o cose el canal para cerrarlo y repara de esta manera el anillo muscular. En los adolescentes y adultos EL TRATAMIENTO ES una cirugía, y por lo general se usa una prótesis o malla que cubre el defecto.
¿Cómo se trata un hidrocele?
En los casos en que el hidrocele causa síntomas como crecimiento o un cambio de tamaño importante durante el día, es necesaria la reparación quirúrgica. Si el hidrocele no presenta complicaciones, se hace una incisión en el escroto. El hidrocele se extirpa, quitando todos los tejidos involucrados. Si hay complicaciones, como una hernia, se hace una incisión en el área inguinal (ingle). Este abordaje permite la reparación de las hernias y de otros factores que pueden complicar el cuadro, al mismo tiempo.
¿Qué se puede esperar después del tratamiento de una hernia o de un hidrocele?
Una vez realizada la cirugía, el paciente se sentirá incómodo y necesitará medicamentos contra el dolor. En la mayoría de los casos, el dolor mejora durante la primera semana y entonces no es necesario tomar medicamentos contra el dolor. Dependiendo de la edad del niño y de si fue operado de uno o de los dos lados, puede ser necesario restringir el desarrollo normal de actividades durante varias semanas, pero esto depende de la edad del niño y de la naturaleza del tratamiento (se realizó el tratamiento en un solo lado o en los dos lados). Si su hijo todavía juega con juguetes de montar, como un caballo mecedor, tal vez sea conveniente que no los use por un tiempo. El testículo y el escroto pueden permanecer inflamados por varias semanas después de la cirugía antes de volver a su estado normal. Luego de la cirugía, menos del 1 por ciento de los casos presentan una recidiva de la hernia o del hidrocele.
Preguntas frecuentes:
¿La hernia y el hidrocele son enfermedades hereditarias?
No. Las hernias y los hidroceles son enfermedades que se presentan con frecuencia. Y si bien varios integrantes de una familia pueden experimentarlos, no hay evidencia de que sean hereditarios.
¿Hay algo que pueda haber hecho alguno de los padres para ocasionar la hernia o el hidrocele en su hijo?
No.
¿Cuál es la posibilidad de que una hernia se desarrolle del otro lado?
Esto depende de la edad del niño. Los niños más jóvenes tratados por una hernia tienen una mayor probabilidad de desarrollar una hernia del otro lado que los niños mayores. En los niños más jóvenes, a veces se utiliza un laparoscopio para observar el otro lado y evaluarlo. Si el examen muestra que ya existe una hernia o que es probable que se desarrolle una, entonces se hace una reparación quirúrgica de los dos lados como una medida de acción preventiva.
¿Cuál es la posibilidad de que una hidrocele se desarrolle del lado contrario?
El riesgo de desarrollar un hidrocele del otro lado es de alrededor del 5 por ciento. Como es un riesgo bajo, muchas veces no se realiza la evaluación por laparoscopía.
¿Las niñas pueden presentar un hidrocele o una hernia?
Las niñas no desarrollan hidroceles. Sí pueden presentar hernias, pero debido a su anatomía, las niñas son 10 veces menos propensas que los niños a desarrollar una hernia.
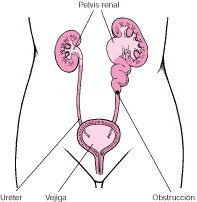
Infecciones del tracto urinario
¿Cuáles son los síntomas de una infección del tracto urinario?
Cuando ocurre una infección del tracto urinario (ITU), el revestimiento de la vejiga y de la uretra se enrojece e irrita de la misma manera que ocurre con la garganta al contraer un resfrío. La irritación puede causar dolor en el abdomen y en el área de la pelvis y puede ocasionar una sensación de necesidad de vaciar la vejiga con mayor frecuencia. Incluso puede intentar orinar y eliminar sólo unas cuantas gotas de orina y/o sentir un dolor urente cuando la orina sale. A veces es posible que pierda el control de la orina. También puede notar que la orina tiene un olor desagradable o que se encuentra turbia.
Las infecciones renales a menudo generan fiebre y causan dolor en la espalda. Estas infecciones deben tratarse con rapidez porque una infección en los riñones puede diseminarse rápidamente al flujo sanguíneo y generar una enfermedad potencialmente letal.
Las ITU a menudo se clasifican como simples (no complicadas) o complicadas. Las ITU simples son infecciones que ocurren en tractos urinarios normales. Las ITU complicadas ocurren en tractos urinarios anormales o cuando las bacterias que causan la infección son resistentes a muchos de los medicamentos antibióticos.
¿Cuáles son las causas de las infecciones del tracto urinario?
Hay grandes cantidades de bacterias que viven en el área rectal y también sobre la piel. Es posible que bacterias de la uretra logren pasar a la orina y viajen hasta la vejiga. Pudiendo, incluso, llegar a los riñones. Pero independientemente de cuán lejos lleguen, las bacterias en el tracto urinario pueden causar problemas.
De la misma manera que algunas personas son más propensas a contagiarse de un resfrío, hay personas que son más propensas a desarrollar una ITU. Las mujeres que han pasado por la menopausia tienen un cambio en el revestimiento de la vagina y pierden los efectos protectores del estrógeno que disminuye la probabilidad de sufrir una ITU. Las mujeres posmenopáusicas que tienen una ITU pueden beneficiarse con el tratamiento de reemplazo de hormonas. Algunas mujeres tienen una predisposición genética a desarrollar una ITU y tienen un tracto urinario que permite a las bacterias adherirse con más facilidad. La actividad sexual también aumenta la frecuencia de las ITU.
Se ha encontrado que las mujeres que usan diafragmas también presentan un mayor riesgo al compararlas con las que usan otras formas de control de la natalidad. El uso de condones con espermicida también está asociado con un aumento de las ITU en el sexo femenino. Las mujeres son más propensas a las ITU porque tienen uretras más cortas que los hombres, entonces las bacterias deben recorrer una distancia más corta para llegar a la vejiga.
Las probabilidades de contraer una ITU son mayores si el tracto urinario tiene una anomalía o si ha sido sometido a algún procedimiento de manera reciente (por ejemplo, colocación de una sonda). Si no puede orinar normalmente a causa de algún tipo de obstrucción, las probabilidades de desarrollar una ITU también son mayores.
Ciertas enfermedades como la diabetes también ponen a las personas en un mayor riesgo de contraer una ITU a causa de la disminución de la función inmunológica del cuerpo, lo que ocasiona una menor capacidad de combatir infecciones como las ITU.
Las anomalías anatómicas en el tracto urinario también pueden llevar a una ITU. Estas anomalías a menudo se encuentran en niños de corta edad, pero también pueden encontrarse en adultos. Pueden haber anomalías estructurales, como bolsas que sobresalen de la pared, llamadas divertículos, y que alojan bacterias en la vejiga o en la uretra, o incluso bloqueos, como la vejiga agrandada, que reducen la capacidad del cuerpo de eliminar la orina de la vejiga por completo.
¿Cómo se diagnostican las infecciones del tracto urinario?
Si piensa que puede tener una ITU, debe consultar a su médico. Con frecuencia es posible hacer un diagnóstico y aplicar el tratamiento sin necesidad de ir al consultorio médico. Las formas de diagnóstico de una ITU son el análisis de orina y/o un cultivo urinario. Se examina una muestra de orina bajo microscopio en busca de indicios de infección, como las bacterias o la presencia de glóbulos blancos en la orina. El médico también puede indicar un cultivo de orina si lo considera necesario. Si alguna vez observa sangre en su orina, debe consultar a su médico de inmediato. La presencia de sangre en la orina puede deberse a una ITU, pero también puede estar indicando otro problema en el tracto urinario.
Si tiene fiebre y presenta los síntomas de una ITU, o si los síntomas persisten a pesar del tratamiento, se recomienda que lo atienda un médico. Tal vez necesite hacerse más estudios, como una ecografía o una tomografía computarizada, para evaluar el tracto urinario.
¿Cómo es el tratamiento de las infecciones del tracto urinario?
Una ITU simple puede tratarse con un esquema corto de antibióticos por vía oral. Un esquema de tres días con antibióticos normalmente será suficiente para tratar la mayoría de las ITU no complicadas. Sin embargo, algunas infecciones pueden requerir un tratamiento de varias semanas de duración. De acuerdo al tipo de antibiótico utilizado, puede tomar una única dosis de medicamento por día o hasta cuatro dosis diarias. Unas cuantas dosis de medicamento pueden aliviar el dolor y la urgencia para orinar con frecuencia, pero debe completar el ciclo completo con el medicamento que le recetaron incluso aunque hayan desaparecido todos los síntomas. A menos que la ITU se trate por completo, suele recidivar con frecuencia. También debe recordar ingerir muchos líquidos, especialmente si tiene una ITU.
Si la ITU es del tipo complicado, entonces es necesario extender el período de tratamiento con antibióticos, y normalmente se comienza por vía intravenosa en el hospital. Luego de un corto período de antibióticos por vía intravenosa, se pasa a antibióticos por vía oral durante un período de hasta varias semanas de duración. Las infecciones renales normalmente se tratan como una ITU complicada.
¿Qué se puede esperar luego del tratamiento de las infecciones del tracto urinario?
Una ITU simple mejora casi siempre con los tres días de tratamiento con antibióticos por vía oral y no es necesario hacer un cultivo de orina para probar que se ha erradicado. No obstante, con una ITU complicada es necesario hacer un cultivo de orina para probar que la ITU se ha ido. Si los síntomas continúan incluso con la medicación, entonces tal vez necesite un esquema de tratamiento más prolongado, un fármaco diferente o una forma de administración diferente (por ejemplo, si está tomando los medicamentos por vía oral, tal vez necesite que se los administren por vía intravenosa).
Preguntas frecuentes:
¿Una ITU puede dañar los riñones?
Si la ITU se trata de manera temprana, entonces probablemente no tenga una influencia duradera sobre el tracto urinario. Si la ITU es recurrente o no se detecta a tiempo puede causar daños si no se remedia en forma rápida.
¿Por qué contraigo ITUs?
La mayoría de las ITUs son eventos aislados que, si reciben tratamiento, no son recidivantes. Algunos pacientes tienen predisposiciones genéticas y anatómicas que tienden a hacer que sean más susceptibles que otras personas.
¿Cómo puedo evitar una ITU?
Hay algunos pasos simples que las mujeres pueden aplicar para evitar una ITU: Las mujeres que ya han pasado por la menopausia y que han perdido la producción normal de estrógeno presentan algunas modificaciones en el revestimiento que recubre a la vagina. El reemplazo hormonal con estrógeno con la orientación de un ginecólogo, un médico de atención primaria, o ambos, puede ser una solución simple. Como algunas pacientes no pueden recibir reemplazo hormonal con estrógeno, es necesario que consulte a su médico antes de comenzar a utilizarlo.
La micción luego de la actividad sexual también puede reducir el riesgo de ITU porque puede eliminar las bacterias que se puedan haber introducido durante el acto sexual. A veces una dosis de antibióticos luego de la actividad sexual puede ayudar a prevenir la recidiva de una ITU.
Ciertas formas de control de la natalidad como los espermicidas y los diafragmas pueden aumentar el riesgo de contraer una ITU en las mujeres que los utilizan como método anticonceptivo.
También debe beber mucho líquido para tener una buena hidratación.
No debe demorar la micción y no debe orinar apurada. La retención de orina y el hecho de no vaciar por completo la vejiga también puede aumentar el riesgo de sufrir una ITU.
Debe limpiar desde adelante hacia atrás para evitar que las bacterias de la zona del ano ingresen a la vagina o a la uretra.
¿Cuándo debo preocuparme?
Si tiene síntomas de una ITU y está recibiendo tratamiento y no observa una mejoría de los síntomas, o si tiene síntomas de una ITU acompañados de náuseas y vómitos, entonces debe consultar un médico. Si alguna vez observa sangre en su orina, debe consultar a su médico de inmediato.
¿Qué ocurre si estoy embarazada?
Si está embarazada y tiene los síntomas de una ITU debe consultar a su médico de inmediatamente. Una ITU durante el embarazo puede poner tanto a la madre como al bebé en riesgo si no se trata de manera rápida y adecuada.
¿Si la ITU es recidivante, puedo superarla?
Si tiene varios episodios de ITU recidivante (tres o más por año), entonces debe consultar a su médico para hacer algún estudio como un análisis de orina. También puede ser necesario realizar una ecografía o una tomografía computarizada para controlar que no haya anomalías en el tracto urinario. Si continúa teniendo episodios de ITU, puede beneficiarse con un esquema más prolongado de antibióticos o tomando un antibiótico luego de la actividad sexual. También hay métodos de autoanálisis que puede coordinar con la ayuda de su urólogo para poder hacer tanto el diagnóstico como el tratamiento de las ITU en su casa.
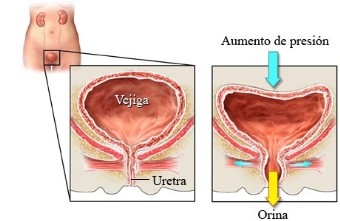
Tratamiento quirúrgico de la incontinencia urinaria
El control de la micción es un problema habitual pero complejo que puede afectar seriamente la vida de una persona. Afortunadamente, con los procedimientos actuales de alta tecnología y los potentes fármacos disponibles, este diagnóstico simplemente puede significar que el camino hacia el control de la micción es un desafío pero no es imposible. Le recomendamos que lea la información que sigue para aprender más acerca de las opciones de tratamiento disponibles, de manera de estar mejor preparado al hablar con su urólogo.
¿Qué se puede esperar en condiciones normales?
El tracto urinario es similar a un sistema de plomería, con caños especiales que permiten que el agua y las sales fluyan a través de ellos. El tracto urinario incluye dos riñones, dos uréteres, la vejiga y la uretra.
Los riñones actúan como sistema de filtrado para la sangre, dado que eliminan los materiales tóxicos y retienen a los elementos útiles como la glucosa, las sales y los minerales. La orina es el producto de desecho del filtrado, se produce en los riñones y fluye a través de dos tubos de 10 a 12 pulgadas de largo (25,4 - 30,5 cm) llamados uréteres, que conectan a los riñones con la vejiga. Los uréteres tienen aproximadamente un cuarto de pulgada de diámetro (0,6 cm) y sus paredes musculares se contraen para dar lugar a la formación de movimientos en forma de ondas que obligan a la orina a ir hasta la vejiga. La vejiga es un órgano que se puede expandir y almacena la orina hasta que se pueda eliminar. Ademàs posee válvulas unidireccionales de cierre que permiten el flujo de orina hacia el interior de la vejiga pero impiden que la orina regrese hacia los riñones (reflujo vesicoureteral). El tubo a través del cual la orina es eliminada del cuerpo se denomina uretra.)
¿Qué es la incontinencia urinaria?
La incontinencia urinaria es la pérdida involuntaria de orina. No es una enfermedad, sino más bien un síntoma que puede deberse a una amplia variedad de enfermedades. La incontinencia puede ser causada por diabetes, accidente cerebrovascular, esclerosis múltiple, enfermedad de Parkinson, algunas cirugías o incluso durante la maternidad. Más de 15 millones de personas en los Estados Unidos, principalmente mujeres, sufren de incontinencia urinaria. Si bien es más habitual en mujeres mayores de 60 años, puede ocurrir a cualquier edad. La mayoría de los profesionales de los servicios sanitarios clasifican a la incontinencia por los síntomas o circunstancias en las que ocurre. En la población normal, la incidencia de incontinencia en las mujeres de más de 65 años es de más del 25 por ciento, en comparación con alrededor del 15 por ciento en los hombres.
¿Cuáles son los diferentes tipos de incontinencia urinaria?
Incontinencia de esfuerzo: La incontinencia urinaria por esfuerzo es la causa más común de pérdida de orina. Ocurre cuando se pierde orina durante actividades como caminar, hacer ejercicios aeróbicos o incluso estornudar y toser. La mayor presión abdominal asociada con estos eventos hace que la orina se escape. Los músculos del piso de la pelvis, que dan soporte a la vejiga y a la uretra, pueden estar debilitados, y de esta manera impiden que los músculos del esfínter funcionen correctamente. Esto también puede ocurrir si los músculos del esfínter en sí están debilitados o dañados a causa de traumatismos quirúrgicos o de partos previos. Las mujeres en la menopausia también pueden sufrir de pequeñas cantidades de pérdida de orina como resultado de los menores niveles de estrógeno. En los hombres, la causa más común de incontinencia son los procedimientos quirúrgicos en la próstata. Ocurre con más frecuencia luego de una prostatectomía radical a causa de cáncer que luego de una cirugía transuretral por HPB.
Incontinencia por necesidad urgente de orinar: También conocida como "vejiga hiperactiva", la incontinencia por necesidad urgente de orinar es otra forma de pérdida de orina. Puede ocurrir cuando una persona tiene una urgencia incontrolable por orinar pero no puede llegar al baño a tiempo y como consecuencia sufre la pérdida de orina. En otras oportunidades, el evento puede estar causado por agua que corre o por las bajas temperaturas. Algunas personas no reciben advertencia y experimentan las pérdidas de orina simplemente al cambiar la posición del cuerpo (por ejemplo al levantarse de la cama). La vejiga hiperactiva también se asocia con accidentes cerebrovasculares, esclerosis múltiple y lesiones en la médula espinal.
Incontinencia por rebosamiento: Este tipo de incontinencia ocurre cuando la vejiga está llena y no puede vaciarse, lo que produce la pérdida de orina. Los síntomas son las micciones pequeñas y frecuentes y el goteo constante. Este tipo de incontinencia no es común en mujeres, y es más común en hombres que han sido sometidos a alguna cirugía o que tienen problemas de próstata.
Incontinencia funcional: Este tipo de incontinencia se debe a la incapacidad para acceder de manera adecuada a un establecimiento o baño a causa de una discapacidad física o mental.
Incontinencia mixta: La incontinencia mixta se refiere a la combinación de más de un tipo de incontinencia, comúnmente incontinencia por estrés e incontinencia por necesidad urgente de orinar.
¿Cómo se hace el diagnóstico?
Al igual que con cualquier otro problema clínico, es muy importante la confección de una buena historia clínica y del examen físico. El urólogo primero hará preguntas acerca de los hábitos individuales y de la ingesta de líquidos, así como acerca de los antecedentes clínicos, quirúrgicos y familiares. Se hará un examen de pelvis exhaustivo en busca de motivos corregibles de la pérdida de orina, entre los que se incluyen el impacto fecal, la constipación y las hernias. Normalmente en la primera evaluación se hará un análisis de orina y una prueba de estrés provocando la tos. Si alguno de los hallazgos sugiere que puede ser necesaria una evaluación más detallada, se puede recomendar la realización de otros estudios como una cistoscopia o incluso un estudio urodinámico. Estos estudios que se realizan de manera ambulatoria normalmente se hacen mediante la inserción de una pequeña sonda en la vejiga a través de la uretra y a veces también con una pequeña sonda rectal.
¿Cuáles son algunas de las opciones de tratamiento para cada tipo de incontinencia?
En la mayoría de los casos de incontinencia se indica un tratamiento mínimamente invasivo (manejo de los líquidos, entrenamiento de la vejiga, ejercicios de los músculos del piso de la pelvis y medicamentos). Sin embargo, si esto fracasa puede ser necesario un tratamiento quirúrgico.
Incontinencia por de esfuerrzo: Uno de los tratamientos quirúrgicos para esta enfermedad en los hombres es el uso de inyecciones uretrales de agentes volumétricos para mejorar la función del esfínter. Las inyecciones se aplican bajo anestesia local y pueden repetirse. Desafortunadamente la tasa de curación sólo es de un 10 a un 30 por ciento. Otra alterativa es realizar un procedimiento de compresión de la uretra con un injerto vascular o un segmento de tejido cadavérico para comprimir la uretra en el área entre el escroto y el recto. Los resultados se encuentran aún en etapa muy preliminar y este tratamiento en la actualidad se realiza sólo en forma experimental. El tratamiento más efectivo para la incontinencia en los hombres es el implante de un esfínter artificial. El dispositivo se inserta debajo de la piel y consiste en un manguito de presión alrededor de la uretra, un balón lleno de líquido que regula la presión en el abdomen y una bomba en el escroto que es controlada por el paciente. El líquido presente en el balón abdominal es transferido al manguito de presión de la uretra, cerrándola y evitando así la pérdida de orina.
La incontinencia por estrés en las mujeres se trata en sus inicios con la modificación del patrón de comportamiento y ejercitación de la pelvis. Hay algunas técnicas que pueden ayudar, como la biorretroalimentación o la estimulación eléctrica de los músculos de la pelvis. Pero cuando los síntomas son más graves y las medidas conservadoras no ayudan, el tratamiento es la cirugía. En algunos casos es posible utilizar agentes volumétricos para aumentar la continencia. La operación se hace con anestesia local y es mínimamente invasiva, pero las tasas de curación son bajas en comparación con las de los procedimientos quirúrgicos a cielo abierto.
La reparación anterior (plicatura de Kelly) es una opción que habitualmente usan los ginecólogos pero que no ha dado buenos resultados a largo plazo. Otra opción es la cirugía abdominal (suspensión de Burch) en la que los tejidos vaginales se fijan al hueso del pubis. Los resultados a largo plazo son buenos, pero la cirugía requiere un mayor tiempo de recuperación y generalmente sólo se usa cuando se requieren otras cirugías abdominales. La cirugía más común y la más popular para la incontinencia por estrés es el procedimiento del cabestrillo. En esta operación se aplica una cinta de tejido debajo de la uretra para proporcionar compresión y mejorar el cierre de la uretra. La operación es mínimamente invasiva y los pacientes se recuperan con mucha rapidez. El tejido utilizado para crear el cabestrillo puede ser un segmento de la pared abdominal del paciente, especialmente fascia tratada, piel de un cadáver o un material sintético.
Incontinencia por necesidad urgente de orinar: Para la incontinencia por urgencia hay una gran variedad de opciones de tratamiento. El primer paso debe ser la modificación del comportamiento: beber menos líquidos; evitar la cafeína, el alcohol y los condimentos; no beber antes de acostarse y orinar periódicamente y no esperar a último momento. La ejercitación de la musculatura del piso pelviano también es útil (ejercicios de Kegel). Es importante mantener un registro de la frecuencia de la micción, la cantidad de episodios de pérdida de orina, la cantidad de orina perdida, la ingesta de líquidos y, si se utilizaran, la cantidad de tohallas higienicas usadas. La base del tratamiento para la vejiga hiperactiva son los medicamentos. Consiste en el uso de relajantes que evitan que la vejiga se contraiga sin que el paciente lo permita. Los efectos colaterales más comúnes de estos medicamentos son la sequedad en la boca, la constipación y las alteraciones en la visión. A veces los efectos colaterales desaparecen al reducir la dosis del medicamento.
Es posible considerar otras alternativas en pacientes que no responden a la modificación del patrón de comportamiento, a la medicación, o a ninguno de ellos. Hay una nueva y prometedora tecnología que consiste en el uso de un marcapasos vesical para controlar el funcionamiento de la vejiga. Esta tecnología consiste en un pequeño electrodo que se inserta en la espalda del paciente cerca del nervio que controla la función de la vejiga. El electrodo se conecta a un generador de pulsos y los impulsos eléctricos controlan la función de la vejiga. Con esta tecnología se logra más de un 60 a un 75 por ciento de cura o mejoría. En los casos más complicados, la vejiga puede agrandarse utilizando un segmento del intestino delgado. Esta operación, llamada cistoplastia de agrandamiento, es muy exitosa para curar la incontinencia pero su principal desventaja es la necesidad de realizar autocateterizaciones para vaciar la vejiga en un 10 a un 30 por ciento de los pacientes.
Incontinencia por rebosamiento: En el caso de la incontinencia por rebosamiento el tratamiento es vaciar completamente la vejiga y evitar que se pierda orina. Los pacientes con vejiga diabética o los pacientes con obstrucción prostática a menudo desarrollan este tipo de incontinencia. La incontinencia por rebosamiento ocasionada por una obstrucción debe tratarse con medicamentos o cirugía para eliminar la obstrucción. Si no se encuentra ninguna obstrucción, el mejor tratamiento es dar instrucciones al paciente para que realice autocateterizaciones varias veces al día. Al vaciar la vejiga con cierta regularidad la incontinencia desaparece y se protege a los riñones.
¿Qué se puede esperar luego del tratamiento?
El objetivo de cualquier tratamiento para la incontinencia es mejorar la calidad de vida del paciente. En la mayoría de los casos es posible lograr grandes mejoras e incluso la curación de los síntomas. El tratamiento médico normalmente es eficaz, pero esto no ocurre si el paciente bebe líquidos durante todo el día y no controla sus horarios para orinar. De manera similar, los grandes aumentos de peso y las actividades que promueven el esfuerzo abdominal ponen a prueba cualquier reparación que se haya logrado y no es probable que resista el paso del tiempo. Si se aplica sentido común, una mecánica corporal adecuada y se tiene cuidado es casi seguro que se lograrán resultados positivos y a largo plazo.
El tratamiento médico de la vejiga hiperactiva (urgencia e incontinencia por necesidad urgente de orinar) puede ser muy exitoso, pero hay factores que pueden afectar negativamente la eficacia del tratamiento, por ejemplo una cirugía previa, la falta de hormonas, las enfermedades neurológicas y la edad. Hay complicaciones leves a causa del tratamiento con medicamentos, que incluyen la constipación y la sequedad en la boca, que algunos pacientes no pueden tolerar. La cirugía, como la inserción de un marcapasos vesical, puede resultar en un 50 a un 70 por ciento de curaciones o una mejoría más importante de los síntomas. El agrandamiento de la vejiga mediante el uso de un segmento de intestino puede curar la incontinencia por necesidad urgente de orinar en más del 80 por ciento de los casos, pero la principal desventaja es la necesidad de realizar autocateterizaciones por el resto de sus vidas en un 10 a un 30 por ciento de los pacientes. A veces ésta es la única opción cuando todos los demás tratamientos han fracasado.
La cirugía para corregir la incontinencia urinaria en los hombres, como la del esfínter artificial, puede curar o mejorar en forma significativa a más del 70 al 80 por ciento de los pacientes. Los resultados pueden verse negativamente afectados por el tratamiento previo con sesiones de radiación, el mal funcionamiento de la vejiga y/o la presencia de tejido cicatrizal en la uretra. Al ser un dispositivo mecánico, puede requerir reparaciones con el tiempo.
La cirugía para corregir la incontinencia urinaria (incontinencia de esfuerzo) en las mujeres es en general muy exitosa, pero es importante la elección del procedimiento adecuado. Muchas pacientes con incontinencia por estrés también presentan otras enfermedades como prolapso vesical, rectocele o prolapso uterino que deben tratarse al mismo tiempo. La combinación de los síntomas de la incontinencia por necesidad urgente de orinar requiere primero un tratamiento médico que intente mejorar los síntomas. El procedimiento de elección dependerá de varios factores, como la necesidad de cirugía abdominal para otras enfermedades, el grado de incontinencia, el grado de movilidad de la uretra y de la vejiga y la experiencia personal del cirujano. En casos simples de incontinencia por estrés con movilidad uretral leve a moderada, el procedimiento de elección es el cabestrillo. El paciente puede esperar un 80 a un 90 por ciento de probabilidades de cura o una gran mejoría. Hay agentes inyectables que pueden curar a un 30 por ciento de los pacientes, pero pueden requerir aplicaciones múltiples.
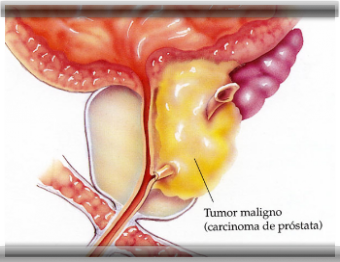
Tratamiento quirúrgico del cáncer de próstata
El cáncer de próstata es una de las formas más comunes de cáncer en los hombres. Unos 200,000 hombres en los Estados Unidos reciben el diagnóstico de cáncer de próstata por año, y unos 32,000 mueren anualmente a causa de esta enfermedad. En las décadas recientes ha habido un aumento constante en la incidencia del cáncer de próstata, pero los médicos están haciendo progresos en el tratamiento y las tasas de supervivencia están mejorando. ¿Cuáles son los síntomas? ¿Cómo saber si la cirugía es el tratamiento que más le conviene? La siguiente información debería resultarle útil para hablar con un urólogo acerca de esta enfermedad.
¿Qué ocurre en condiciones normales?
La glándula prostática tiene aproximadamente el tamaño de una nuez. Está ubicada entre la vejiga y el pene, y rodea a la uretra. La glándula prostática es parte del sistema reproductor masculino. La función primaria de la glándula es producir y secretar el líquido eyaculatorio.
¿Qué es el cáncer de próstata?
Es una enfermedad que afecta las células de la próstata. Ocurre cuando el proceso normal de crecimiento celular dentro de la próstata se vuelve anormal a causa de una masa de tejido llamada tumor. Al igual que muchos cánceres, la causa del cáncer de próstata es desconocida. Pero los médicos saben que es más común en hombres afro-americanos con antecedente familiar de la enfermedad. La hormona sexual masculina testosterona también contribuye al crecimiento. El cáncer de próstata es muy común, cada hombre tiene una posibilidad entre seis de desarrollar cáncer de próstata en su vida. En la actualidad, gracias al amplio conocimiento de los estudios que se pueden realizar para el estudio de la próstata, alrededor de un 80 por ciento de los hombres en los que se encuentra un cáncer de próstata tienen la enfermedad aparentemente confinada a la próstata y por lo tanto responden bien a los tratamientos, incluida la cirugía.
¿Cuáles son los síntomas del cáncer de próstata?
En sus primeras etapas, el cáncer de próstata puede ser asintomático. Pero a medida que progresa pueden aparecer los siguientes síntomas: micción frecuente (especialmente durante la noche), problemas para orinar (incapacidad, flujo débil, dolor, ardor, etc.), eyaculación con dolor, sangre en la orina o en el semen y/o dolor frecuente y rigidez en la espalda, en las caderas o en la parte superior de los muslos.
¿Cómo se diagnostica el cáncer de próstata?
En el caso ideal, el cáncer de próstata se detecta cuando es tan pequeño que no hay ningún síntoma. La detección temprana se puede lograr mediante un tacto rectal (TR) y un estudio del PSA, que puede llevar al médico a pedir una biopsia de próstata. Para esta biopsia se utiliza una sonda ecográfica que se inserta en el recto y una aguja para biopsia que se dirige a diferentes áreas de la glándula prostática.
Una vez que se ha diagnosticado el cáncer de próstata a partir de una biopsia de la próstata, el médico clasifica la enfermedad de acuerdo a su estadio para determinar la extensión del cáncer y para determinar si se ha extendido a los ganglios linfáticos y/o a los huesos.
Para determinar si el cáncer se ha diseminado a los ganglios linfáticos o a los huesos, el médico puede pedir que se haga una tomografía computarizada de la pelvis o de los huesos.
Además de los estadios, el médico busca determinar la "agresividad" del cáncer. Esto se puede hacer de dos maneras. La primera es determinando el grado del cáncer; es decir, cuán "agresivo" se ve bajo el microscopio. El sistema más utilizado para clasificar el cáncer de próstata es el sistema Gleason, que asigna valores de entre dos y 10 al cáncer. Los valores entre dos y cuatro indican poca agresividad, los valores entre cinco y seis indican una agresividad leve, siete indica agresividad moderada, y los valores de entre ocho y 10 indican que el cáncer es altamente agresivo. El segundo signo para la clasificación de la agresividad es el nivel de PSA antes de la biopsia. En general, lo ideal es que el nivel de PSA sea inferior a 10 ng/ml, si el nivel se encuentra entre 10 y 20 ng/ml es necesario estar un poco más atento al comportamiento de la enfermedad, y los valores por encima de 20 ng/ml son muy preocupantes aunque a veces es posible lograr una curación.
¿Cuándo se recomienda la cirugía para tratar el cáncer de próstata?
En general, la cirugía del cáncer de próstata se realiza en pacientes con la enfermedad en la etapa T1 o T2 (confinada a la glándula prostática) o en una etapa T3 muy pequeña; niveles de PSA inferiores a 20 y puntaje de Gleason menor que ocho. En algunas circunstancias, los pacientes con parámetros más graves pueden ser candidatos a cirugía también. Finalmente, la cirugía del cáncer de próstata normalmente está restringida a hombres que tienen una expectativa de vida de 10 años o más y cuyo estado de salud es suficiente como para resistir los riesgos de una cirugía importante.
¿Cuáles son algunos de los factores de riesgo que se asocian con la cirugía del cáncer de próstata?
Los factores de riesgo de la cirugía son la incontinencia urinaria y la impotencia. La incontinencia es muy poco frecuente, sólo ocurre en menos de un 5 por ciento de todos los casos quirúrgicos. Además, cuando ocurre, hay procedimientos que pueden solucionarla. La impotencia, si aparece después de la cirugía, también puede tratarse con diferentes medicamentos y/o dispositivos técnicos como prótesis penianas.
¿Cuáles son los diferentes tipos de cirugía para el cáncer de próstata?
Prostatectomía retropúbica: Durante este procedimiento, el cirujano hace una incisión a través de la parte baja del abdomen. El cirujano puede resecar la próstata, el tejido circundante y los ganglios linfáticos pelvianos (si es necesario).
Prostatectomía perineal: Durante este procedimiento el cirujano reseca la próstata a través de una incisión en la piel entre el escroto y el ano. En general, la cirugía perineal es un poco más llevadera para el paciente, pero puede ser algo ineficaz si el cáncer es grave, y hay que examinar los ganglios linfáticos antes de resecar la próstata.
Prostatectomía laparoscópica: Este tipo de cirugía elimina la necesidad de una incisión quirúrgica grande para resecar la próstata. Como resultado, el paciente puede sufrir menos dolor y cicatrización, la recuperación es más rápida y el riesgo de infección es menor. Durante este procedimiento se inserta un instrumento telescópico llamado laparoscopio en el abdomen a través de una pequeña incisión en el ombligo. El laparoscopio tiene una cámara que permite a los cirujanos observar dentro del abdomen y realizar la cirugía sin necesidad de hacer una incisión grande. Normalmente se hacen cuatro incisiones pequeñas en el abdomen para acomodar los instrumentos quirúrgicos y se realiza la cirugía. Los pacientes que se hayan sometido a una cirugía previa en la pelvis no son candidatos para este tipo de cirugía.
¿Qué se puede esperar luego del tratamiento quirúrgico?
El paciente comienza la recuperación en el hospital y el dolor se controla con medicamentos. Normalmente para el segundo día se puede retomar una dieta normal. El paciente suele ser dado de alta con una sonda colocada y se le enseña a manejarlo. El catéter se quita usualmente en una visita de control que se hace en el consultorio del cirujano, y el paciente debe comenzar a hacer ejercicios para fortalecer la válvula de control urinario (llamados ejercicios de Kegel). El control urinario (continencia) puede ser inmediato o puede llevar hasta seis meses.
De manera similar, la potencia eréctil puede ser inmediata o la recuperación puede demorarse hasta un año luego de la cirugía. Normalmente, si las erecciones no son suficientes como para poder tener relaciones al mes de la cirugía, se utilizan tratamientos adicionales hasta que las erecciones son suficientes. No se pierde la capacidad de tener un orgasmo. Sin embargo, el orgasmo es "seco" - la eyaculación es muy poca si es que la hay - por lo que la capacidad de procrear normalmente se pierde.
Luego de la cirugía, el cirujano revisa la evaluación final de la próstata resecada (si corresponde) y de los ganglios linfáticos resecados. Sobre la base de esta "patología final", se desarrolla un plan de seguimiento. Si la patología es particularmente grave (por ejemplo, el cáncer se extendió a las vesículas seminales o a los ganglios linfáticos), puede recomendarse un tratamiento adicional. Este tratamiento puede incluir radioterapia y/o tratamiento hormonal. Si la patología no es particularmente grave, el plan de seguimiento incluirá visitas periódicas a un médico y estudios del PSA también periódicos. El nivel de PSA debe ser menor que 0,1 ng/ml. Si es mayor, y especialmente si es mayor que 0,5 ng/ml, el cáncer sigue estando presente y se recomiendan tratamientos adicionales.
Preguntas frecuentes:
¿Cuándo puedo retomar mis actividades normales después de la cirugía?
Es variable, pero normalmente entre tres y seis semanas.
¿Después de la cirugía sabré si estoy curado?
No por completo, y ciertamente varía de acuerdo con la severidad del cáncer resecado. En general, los valores del estudio del PSA deben ser inferiores a 0,1 ng/ml durante diez años para estar seguros de que se logró la cura.
Me preocupa la potencia, pero temo más a la incontinencia.
¿Cuáles son las posibilidades?
Normalmente, la incontinencia es transitoria y no dura mucho, aunque puede persistir por un período de entre seis y nueve meses. Con cirujanos más experimentados, el riesgo de incontinencia permanente es de un 2 a un 5 por ciento luego de la cirugía para el cáncer de próstata.